Sujet zéro série pro
Pour faire face à la pénurie annoncée d'eau potable, de nouvelles techniques de production sont mises en place pour satisfaire les besoins des populations toujours plus nombreuses. Une des techniques prometteuses pour certains pays est le dessalement de l'eau de mer.
On s’intéresse aux deux techniques les plus utilisées pour dessaler l’eau de mer : la distillation et l'osmose inverse .
Document 1 : Présentation de la distillation et de l’osmose inverse.
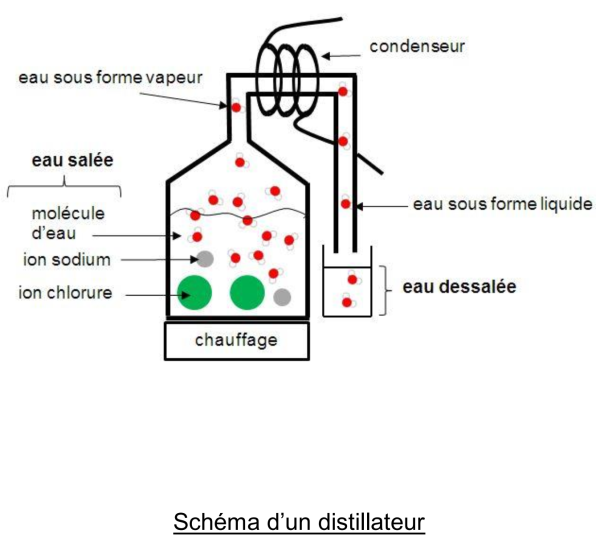
La distillation
Dans les procédés de distillation, il s'agit de chauffer l'eau de mer pour en vaporiser une partie. La vapeur ainsi produite ne contient pas de sels, il suffit alors de liquéfier cette vapeur en la refroidissant à l’aide d’un condenseur, pour obtenir de l'eau douce liquide.
L'inconvénient majeur des procédés de distillation est leur consommation énergétique. En effet pour transformer 1 kg d'eau liquide en 1 kg d'eau vapeur à la même température il faut environ 2 250 kilojoules.
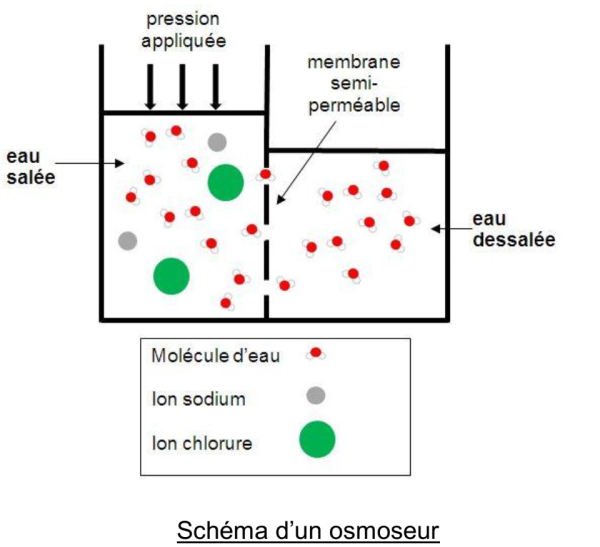
L'osmose inverse
L'osmose inverse est un procédé de séparation de l'eau et des sels dissous au moyen de filtres (membranes semi- perméables). Les membranes laissent passer les molécules d'eau et ne laissent pas passer les sels dissous.
Une station utilisant la technique d’osmose inverse, peut dessaler 10 m3 d’eau de mer par jour.
L'énergie nécessaire vaut environ 20 000 J par kilogramme d’eau traitée.
Rappel : 1 m3 correspond à 1 000 L
D’aprèshttp ://culturesciences.chimie.ens.fr/le-dessalement-de-leau-de-mer-et-des-eaux-saumâtres
Document 2 : Tests de reconnaissance de quelques espèces chimiques
| Formule de l’espèce chimique testée | Réactif | Observation |
|---|---|---|
| Cu2+ | Solution d’hydroxyde de sodium (soude) | Formation d’un solide bleu |
| Fe2+ | Solution d’hydroxyde de sodium (soude) | Formation d’un solide vert |
| Cl- | Solution de nitrate d’argent | Formation d’un solide blanc qui noircit à la lumière |
Question 1 - Dessalement de l’eau de mer.
On considère que l’eau de mer est constituée essentiellement d’eau et de sel (ions chlorure Cl- et ions sodium Na+ ).
En moyenne, un litre d’eau de mer contient une masse de 35 g de sel.
a. À l’aide des données du document 1, calculer la masse de sel récupérée en une journée dans une station utilisant la technique d’osmose inverse.
b. On souhaite vérifier expérimentalement qu’un échantillon d’eau dessalée ne contient plus d’ions chlorure.
Proposer un protocole expérimental à mettre en place. On précisera en particulier les étapes de la manipulation et les observations attendues. On pourra s’aider du document 2, de textes ou de schémas.
Question 2 - Étude de la distillation.
Le diagramme ci-dessous représente les changements d’état ayant lieu lors de la distillation.
a. Nommer les états de l’eau 1 et 2 .
b. Nommer le changement d’état A .
c. En utilisant le document 1 et la relation $t = {\frac E P}$ avec t la durée en secondes, E l’énergie en joules et P la puissance en watts, calculer la durée nécessaire pour distiller 1 kg d’eau de mer si on dispose d’une puissance de chauffage P = 2 300 W.
Question 3
Comparer l’énergie nécessaire pour dessaler 1 kg d’eau de mer par chacune des deux techniques, en s’appuyant sur le document 1.