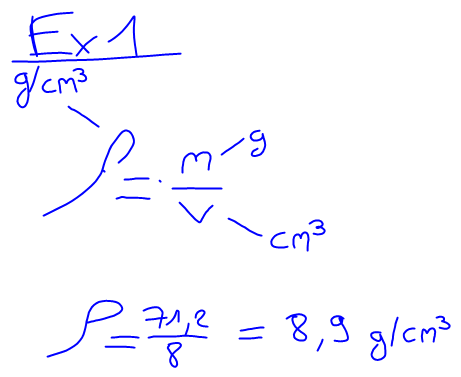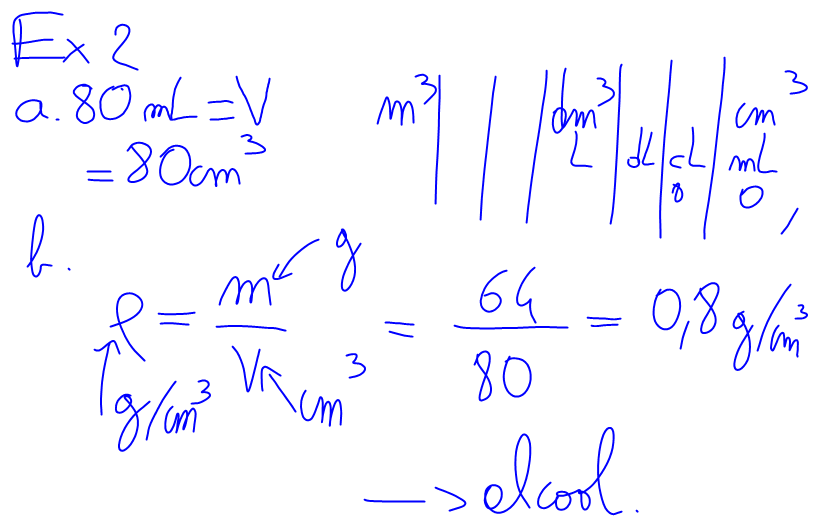Ajouter cette page à votre livre
Retirer cette page de votre livre
Semaine du 21/03/22
1. Correction des exercices sur la masse volumique
2. Leçon
Cliquez pour afficher ⇲
Cliquez pour masquer ⇱
Chapitre I : Les éléments chimiques dans l'Univers
I. La matière
La matière est composée d'atomes. Un atome est électriquement neutre.
Une molécule est un assemblage d'un ou plusieurs atomes.
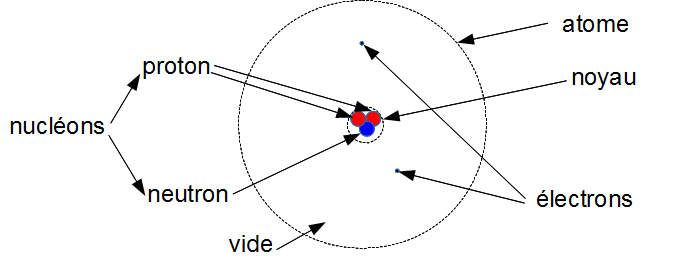
Un atome est composé d'un noyau (chargé positivement) autour duquel tournent des électrons (chargés négativement).
Le noyau est lui-même constitué de nucléons :
- protons (chargés positivement)
- neutrons (neutres)
La taille d'un atome est de l'ordre de 0,1 nm (10-10 m).
Le noyau est 100 000 fois plus petit.
La masse d'un électron est très faible par rapport à celle du noyau. La masse d'un atome est environ égale à celle du noyau.
Il y a principalement du vide dans un atome. On dit qu'il a une structure lacunaire.
II. Quelques exemples
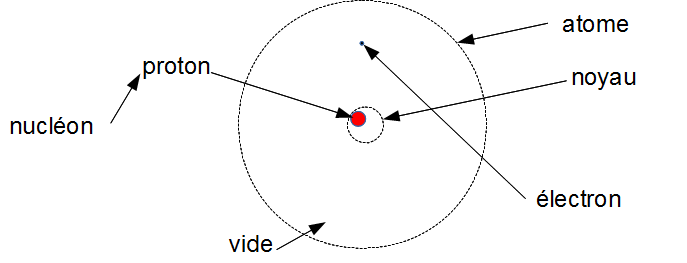
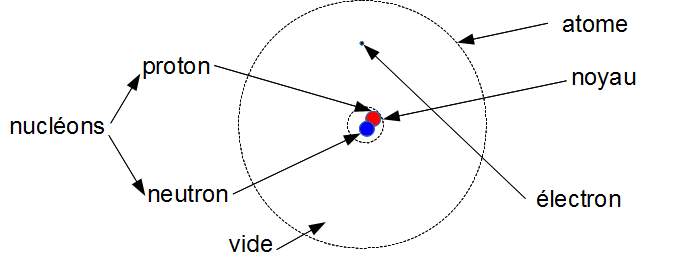
1. Atome d'hydrogène
Son numéro atomique est le 1 donc il y a 1 proton dans le noyau.
Il n'y a pas de neutron dans la plupart des noyaux de atomes d'hydrogène (explication : voir plus loin).
Comme l'atome est neutre, il y a autant de proton (positif) que d'électron (négatif). Il y a donc 1 électron
${{1~électron~(-)} \\ {1~proton~( )}} \\ -> neutre$
Il y a en fait 2 nombre associés à un atome.
$_1^1 H$
Le 2ème nombre correspond au nombre de nucléons dans le noyau. C'est le nombre de masse.
Nombre de nucléons = nombre de protons nombre de neutrons
Si on a $_1^1 H$ cela signifie qu'il y a 1 proton, 1 nucléon donc 1 - 1 = 0 neutron.
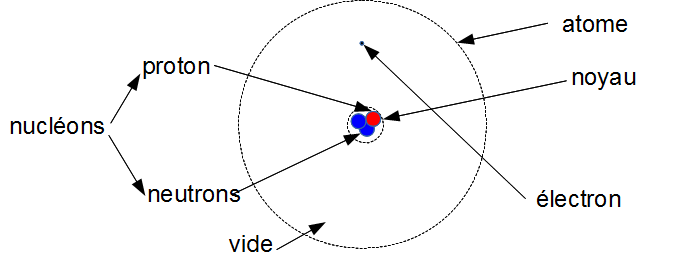
Il existe une autre variété d'hydrogène : $_2^1 H$.
Dans celle-ci il y a donc 1 proton, 2 nucléons, ce qui fait 2 - 1 = 1 neutron
1 proton 1 neutron = 2 nucléons
Une autre variété : $_3^1 H$
Dans celle-ci il y a donc 1 proton, 3 nucléons, ce qui fait 3 - 1 = 2 neutrons
1 proton 2 neutrons = 3 nucléons
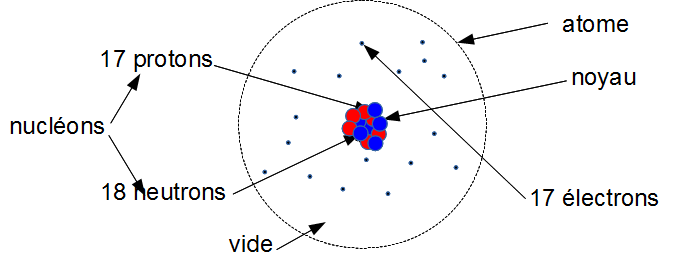
2. Atome de chlore $^{17} Cl$ (c'est la lettre “l” minuscule à coté du C)
- 17 protons (positifs)
- donc 17 électrons
- 18 neutrons pour la variété la plus courante des atomes de chlore
${{17~électrons~(-)} \\ {17~protons~( )}} \\ -> neutre$
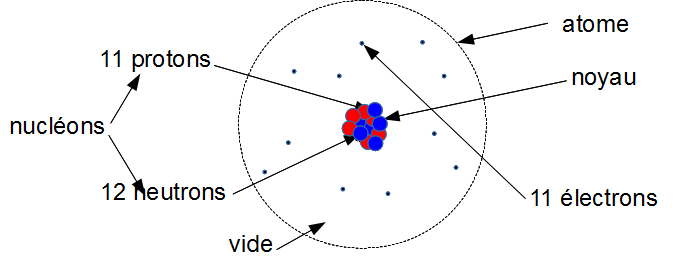
3. Atome de sodium $^{11} Na$
${{11~électrons~(-)} \\ {11~protons~( )}} \\ -> neutre$
Attention, le nombre de neutron n'est pas tout le temps égal au nombre de proton plus un.
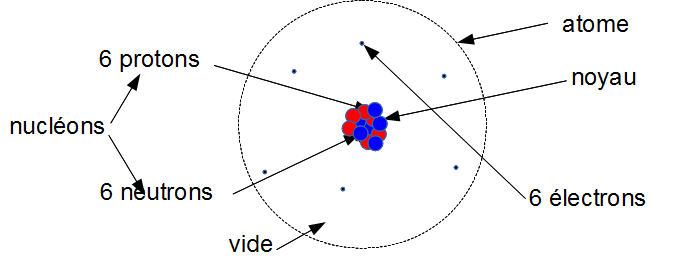
4. Atome de carbone $^{6} C$
${{6~électrons~(-)} \\ {6~protons~( )}} \\ -> neutre$
Pour la petite histoire, il y a généralement 6 neutrons dans l'atome de carbone (donc 12 nucléons) mais il existe une variété radioactive de carbone avec 8 neutrons (donc 14 nucléons). Cette variété s'appelle le carbone 14 et on s'en sert pour dater des objets en histoire ou en archéologie.
3. A faire pour la prochaine fois
Ex 2 4 5 8 p 25 26