Ceci est une ancienne révision du document !
Chp III : Matière et molécules
1. Les molécules
Les molécules sont des particules très petites (de l'ordre du nanomètre 1nm = 10-9m ) constituant la matière.
Un corps pur est constitué de molécules identiques.
Ex : l'eau pure est constituée exclusivement de molécules d'eau.
Un mélange est constitué de molécules différentes.
Ex : l'air est composé de molécules de diazote et de dioxygène.
2. Les états de la matière
2.1. L'état gazeux
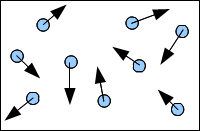
Dans un gaz, les molécules sont éloignées les unes des autres.
Elles bougent de façon désordonnée. Entre les molécules, il y a du vide.
L'état gazeux est dispersé et désordonné.
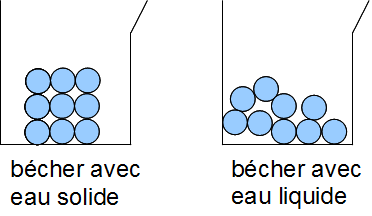
2.2. L'état liquide
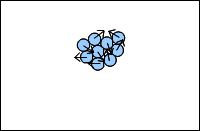
Dans un liquide, les molécules se touchent mais se déplacent les unes par rapport aux autres.
L'état liquide est compact et désordonné.
2.3. l'état solide
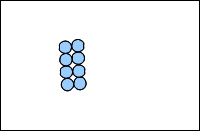
Dans un solide, les molécules se touchent et sont immobiles.
L’état solide est compact ; les solides cristallins sont ordonnés.
3. Comment explique-t-on ...
3.1. La compressibilité d'un gaz
3.2. L'incompressibilité d'un liquide ou d'un solide
Les molécules ne peuvent pas se rapprocher davantage.
Leur nombre ne change pas car la seringue est fermée.
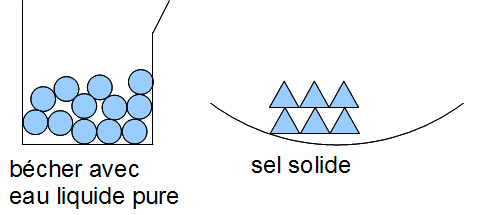
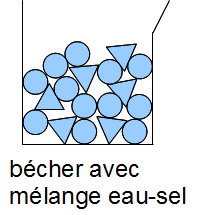
3.3. La conservation de la masse lors des mélanges en solutions aqueuses
On mesure la masse de l'eau et du sel avant le mélange.
On mesure la masse de l'eau salée.
La masse n'a pas varié.
Interprétation :
Le nombre de molécule ne change pas, donc la masse ne change pas non plus.